Obiettivi di apprendimento
- Conoscere le cause più frequenti di oftalmopatia tiroidea
- Saper riconoscere l’aspetto di un paziente con TED
- Inquadramento diagnostico
- Gestione della patologia
Introduzione
L’oftalmopatia tiroidea (TED), precedentemente conosciuta come orbitopatia di Graves, è un esempio importante di malattia autoimmune associata a manifestazioni oculari. Richiede un approccio multidisciplinare e ha un impatto molto importante sulla vita dei pazienti affetti. Il suo tasso di incidenza è di circa 19 su 100000 persone. Si caratterizza da un aumento di volume dei muscoli extra-oculari, grasso orbitario e ghiandola lacrimale dovuto all’azione di autoanticorpi diretti contro recettori tiroidei, che cross-reagiscono localmente.
Epidemiologia
Nel 90% dei casi è una manifestazione clinica del morbo di Basedow-Graves (ipertiroidismo), legata quindi ad una iperattività della ghiandola tiroide; più raramente si associa invece ad una ghiandola tiroide normofunzionante (eutiroidismo) o ipofunzionante (ipotiroidismo come nella tiroidite di Hashimoto).
La TED è più frequente nel sesso femminile, con una prevalenza di 5 volte maggiore rispetto al genere maschile; questo è legato ad una più alta incidenza della malattia di Graves nelle donne. L’età media dei pazienti colpiti è di 43 anni, ma può manifestarsi a qualsiasi età.
Fra i fattori di rischio spicca su tutti il fumo, legato sia all’insorgenza che al peggioramento della condizione clinica. Anche lo stress sembra giocare un ruolo importante nel decorso della patologia.
Fisiopatologia
Anche se il meccanismo esatto non è ancora noto, si presume che la fisiopatologia della TED sia centrata sul ruolo dei fibroblasti orbitari; sulla loro membrana cellulare, infatti, sono espressi i recettori per il TSH e le IGF, target molecolari della risposta autoimmune. Questo legame causa un’attivazione dei fibroblasti orbitari, con successivo deposito di matrice extracellulare (MEC), differenziamento in miofibroblasti o lipofibroblasti, sintesi aberrante di glicosamminoglicani (GAG) e rilascio di TNF-α e IL-6. Il risultato sarà quindi un’infiltrazione infiammatoria locale con richiamo di liquidi e conseguente edema, congestione e rimaneggiamento del tessuto connettivo: questo porta ad un aumento del volume dei muscoli extra-orbitari che in fase avanzata della patologia subiscono una progressiva displasia fibrosa che porta a miopatia restrittiva e diplopia.
Dal momento che l’orbita è una cavità circondata da pareti ossee, quindi non espandibile, l’incremento volumetrico del suo contenuto genera proptosi (una protrusione anomala del bulbo oculare).
Morbo di Basedow-Graves
La malattia di Graves è un disordine autoimmune, caratterizzato dalla presenza di TRab (TSH receptor antibodies, anche noti come TSI: thyroid stimulating immunoglobulines) diretti contro i recettori del TSH, che causano un eccessivo rilascio e produzione di ormoni tiroidei. Come anticipato, l’incidenza nel sesso femminile è circa 5 volte maggiore e presenta un picco bimodale (terza/quarta decade o dopo i 60 anni).
I fattori di rischio riconosciuti possono essere divisi in modificabili e non modificabili:
- Modificabili: fumo, deficit di iodio, deficit di selenio, radiazioni. I pazienti che cessano di fumare hanno una possibilità di recupero durante la terapia 4-5 volte maggiore rispetto a chi continua a fumare.
- Non modificabili: sesso, mutazioni genetiche (CTLA-4, TSHR e tireoglobulina)
La clinica è tipica dell’ipertiroidismo. Il paziente riferisce perdita di peso senza cambi nella dieta abituale, sudorazione e cute calda, nervosismo, tremore e gozzo. Il 25-50% dei pazienti con morbo di Graves sviluppa TED che non è correlata né alla gravità né al timing della disfunzione tiroidea.
La patologia si caratterizza da elevati livelli di T3 e T4 e ridotti livelli di TSH. Nel 98% dei pazienti sono presenti TRab che vanno sempre dosati insieme agli anticorpi anti-tireoperossidasi (anti-TPO).
Nel sospetto quindi di morbo di Graves vanno richiesti i livelli di fT3, fT4, TSH, TRab, Ab anti-TPO; subito dopo questo pannello di esami è opportuno richiedere un’ecografia della tiroide.
Tiroidite di Hashimoto
Anche nota come tiroidite cronica autoimmune, è un processo caratterizzato da una infiltrazione linfocitaria cronica della ghiandola che porta ad una progressiva e irreversibile ipofunzione. Classicamente gli anticorpi che si riscontrano in questa condizione sono gli anti-TPO (95%) e anti-tireoglobulina (50-60%).
Clinica
La TED può presentarsi come unilaterale o bilaterale, simmetrica o asimmetrica, variabile nei giorni e nell’arco della stessa giornata sia nei segni che nei sintomi.
Le manifestazioni caratteristiche a livello oculare sono:
- Retrazione palpebrale
- Coinvolgimento dei tessuti molli
- Proptosi (esoftalmo)
- Alterazioni oculomotorie
- Neuropatia ottica
Decorso della TED
L’oftalmopatia tiroidea presenta un decorso caratteristico:
- Fase attiva di malattia (stadio congestizio o infiammatorio): infiammazione attiva caratterizzata dalla comparsa e dal rapido peggioramento di segni e sintomi fino al raggiungimento di un plateau. Ha una durata variabile tra i 18 e 36 mesi.
- Fase intermedia di malattia: miglioramento graduale fino allo spegnersi della risposta infiammatoria
- Fase tardiva di malattia (stadio fibrotico o quiescente): il quadro clinico si stabilizza (assenza di dolore), ma residuano anomalie sia di tipo funzionale che estetico.
È importante saper identificare la fase della malattia per il management del paziente: la terapia antinfiammatoria trova infatti un razionale solo durante la fase attiva; al contrario, durante il periodo quiescente è possibile mettere in atto interventi di chirurgia correttiva.
Complicanze
Sindrome palpebro-retrattile
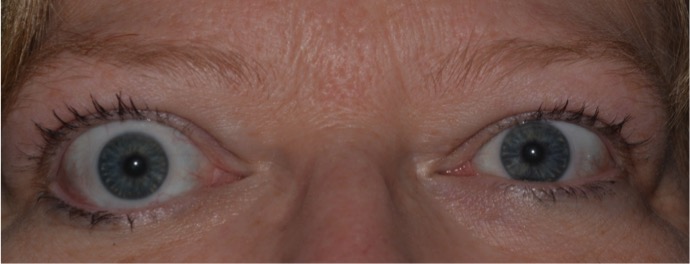
La retrazione palpebrale (segno di Darlymple) è il segno più comune di oftalmopatia tiroidea, presente fino al 90% dei casi. Causa disturbi estetici e funzionali e spesso è il primo segno di ipertiroidismo. Durante la visita è possibile notare una variazione dell’ampiezza palpebrale.
Importante durante la visita annotare:
- Ampiezza della fessura palpebrale: distanza fra il margine palpebrale superiore e inferiore; valori normali sono di circa 7-10 mm nei maschi e 8-12 nelle femmine.
- MRD (Margin to reflex distance): puntando una luce davanti al paziente, la si fa fissare e si misura la distanza che intercorre fra il riflesso luminoso sulla cornea e il margine palpebrale superiore (MRD1) e inferiore (MRD2)
- Scleral show: normalmente il margine palpebrale superiore si trova 2 mm circa al di sotto del limbus (zona di confine fra cornea e sclera), mentre la palpebra inferiore è a circa 1 mm dal limbus. In questi pazienti ci può essere una eccessiva esposizione sclerale.
Le cause della retrazione possono essere legate ad una iperfunzione del muscolo di Müller, (muscolo coinvolto nell’apertura palpebrale, con innervazione simpatica) legata ad un ipertono simpatico negli ipertiroidei; oppure ad una contrazione fibrotica del muscolo elevatore della palpebra o dei muscoli retti inferiori.
È utile in questi pazienti l’esplorazione accurata del comportamento palpebrale durante lo sguardo rivolto verso il basso:
- Se la palpebra superiore rimane retratta si parla di lid lag: indice di scarsa elasticità del muscolo elevatore (fibrosi);
- Se la palpebra superiore segue il movimento del bulbo verso il basso: può esserci una iperfunzione dell’elevatore nello sguardo verso l’alto, dovuto alla resistenza legata alla fibrosi del muscolo retto inferiore.
La sindrome palpebro-retrattile si presenta con altre caratteristiche tipiche nei pazienti con TED:
- Segno di Kocher: descrive un aspetto fisso e spaventato degli occhi
- Segno di Rosenback: tremolio palpebrale alla chiusura, segno dell’ipertono simpatico tipico dell’ipertiroidismo
- Segno di Gifford: difficoltà all’eversione della palpebra superiore
- Segno di Von Graefe: indica una discesa ritardata della palpebra superiore nello sguardo verso il basso, è una asinergia oculo-palpebrale
- Segno di Stellwag: ridotto ammiccamento.
Coinvolgimento dei tessuti molli
Durante la TED c’è un infarcimento infiammatorio a carico di cute, grasso, congiuntiva e ghiandola lacrimale. Il paziente sperimenta discomfort oculare, sensazione di corpo estraneo negli occhi, fotofobia e lacrimazione.
Durante l’esame obiettivo si può evidenziare:
- Chemosi congiuntivale (rigonfiamento edematoso della congiuntiva)
- Iperemia congiuntivale
- Edema della caruncola
- Edema palpebrale con possibile prolasso della ghiandola lacrimale
- Cheratocongiuntivite secca: dovuta ad infiltrazione della ghiandola lacrimale
- Erosioni puntate dell’epitelio corneale: spesso dei settori inferiori, legati a lagoftalmo (incompleta chiusura palpebrale). Fino all’ulcera corneale, unica urgenza oftalmologica insieme alla DON (neuropatia ottica distiroidea, vedi dopo).
Esoftalmo o proptosi
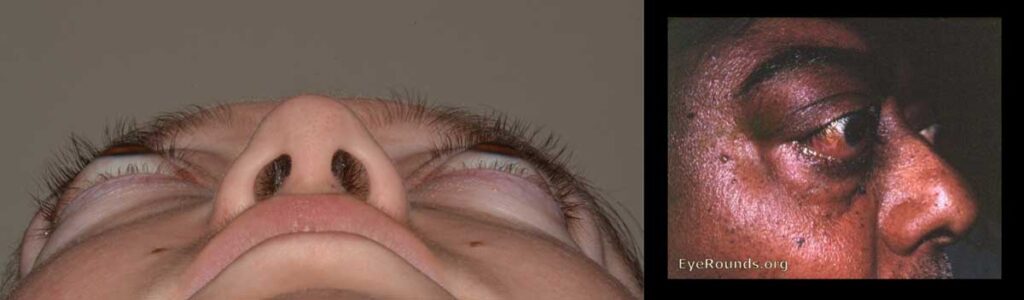
Davanti ad una proptosi bulbare bisogna sempre valutare se è monolaterale o bilaterale, simmetrica o asimmetrica, assile (l’occhio sporge in fuori lungo l’asse visivo) o non assile, riducibile o non riducibile alla digitopressione.
Durante la TED, nel 30-60% dei pazienti, l’esoftalmo in genere è bilaterale, asimmetrico, assile almeno nelle fasi iniziali e riducibile; una proptosi non riducibile deve far pensare a delle masse orbitarie.
Una volta evidenziata la presenza di esoftalmo, è opportuno misurarlo per monitorarlo nel tempo. Si utilizza uno strumento chiamato esoftalmometro di Hertel.
Questo strumento presenta una struttura metallica con 2 alette laterali che vanno appoggiate sulla parete laterale dell’orbita. Va fissata la distanza intercantale (fra il canto medio di entrambi gli occhi) su un righello millimetrato che fa parte della struttura dello strumento. Facendo fissare il paziente in direzione dell’esaminatore, si andrà a misurare l’apice corneale sul righello millimetrato dello specchietto laterale: il valore normale è inferiore o uguale a 20 mm.
È utile annotare tutti i risultati trovati per compararli nelle visite successive.
Alterazioni oculomotorie
Fra il 30 e il 50% dei pazienti presentano una miopatia restrittiva. La motilità oculare viene limitata inizialmente dall’edema infiammatorio, successivamente dalla fibrosi. I muscoli più coinvolti sono il muscolo retto inferiore (60%), il retto mediale (25%) e il retto laterale (10%).
I pazienti manifestano diplopia, inizialmente verticale e in convergenza, successivamente anche nella posizione primaria dello sguardo.
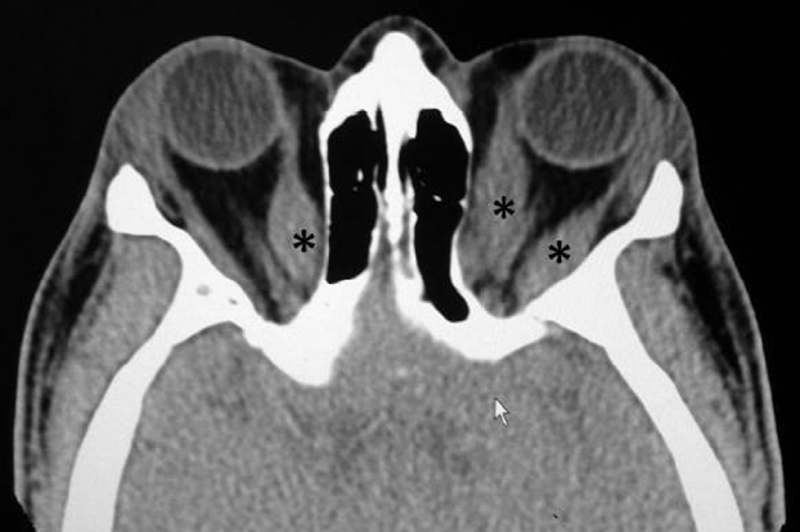
Va tenuto in conto come questa displasia fibrosa coinvolge principalmente il ventre muscolare; questo permette una diagnosi differenziale con le miositi che colpiscono le inserzioni tendinee dei muscoli. La risonanza magnetica ci viene in aiuto.
Neuropatia Ottica Distiroidea (DON)
È una grave complicanza della TED, che si manifesta fino al 6% dei casi. Solitamente è bilaterale e asimmetrica, con insorgenza acuta. Le cause sono riconducibili alla compressione del nervo ottico o della sua vascolarizzazione (con conseguente ischemia) da parte dei muscoli retti congestionati e dei tessuti molli edematosi. Tale compressione può avvenire anche in assenza di esoftalmo significativo, va anzi sottolineato come maggiore è la proptosi, minore è la sofferenza del nervo ottico. Questo è dovuto al fatto che l’esoftalmo riduce l’affollamento dell’orbita, diminuendone quindi la pressione interna.
Clinicamente si presenta con un quadro tipico da coinvolgimento della papilla ottica:
- Edema/iperemia della papilla ottica
- Discomatopsia rosso-verde: il paziente non riesce a distinguere i colori, con desaturazione del rosso
- Alterazione del contrasto
- DPAR: difetto pupillare afferente relativo. La pupilla dell’occhio colpito risulta areagente allo stimolo luminoso; illuminando tuttavia l’occhio controlaterale si otterrà miosi bilaterale.
- Deficit del campo visivo: possono essere centrali o paracentrali
Le forme più a rischio, per quanto detto, sono quelle senza esoftalmo (che risulta infatti essere un meccanismo di decompressione naturale).
La neuropatia ottica in corso di TED necessita di intervento medico o chirurgico di urgenza. Il primo intervento solitamente consiste in boli di metilprednisolone; se la condizione non migliora si valuta la decompressione chirurgica.
Classificazione
Al giorno d’oggi sono due le classificazioni più utilizzate: la CAS (clinical activity score) e quella dell’EUGOGO (European Group on Graves’ Orbitopathy).
La CAS permette di identificare i pazienti con patologia attiva, che potrebbero beneficiare di trattamento medico steroideo. La diagnosi di attività dell’oftalmopatia tiroidea si basa sulla presenza di 3 o più segni basati sulle caratteristiche dei tessuti molli oculari:
- Dolore spontaneo retrobulbare
- Dolore al movimento oculare
- Eritema palpebrale
- Edema palpebrale
- Iperemia congiuntivale
- Chemosi congiuntivale
- Edema della caruncola
Quindi CAS è una classificazione che ci orienta sulla scelta della terapia (come intervenire): medica se la TED è attiva; chirurgica se non è attiva.
La classificazione dell’EUGOGO invece ci permette di stabilire il grado di severità della patologia. Questo risulta importante invece sull’indicazione alla terapia (quando intervenire).
- TED lieve: non influenza la quotidianità. Non giustifica un trattamento immunosoppressivo o chirurgico.
- TED moderata/severa: non ci sono alterazioni visive marcate, ma la malattia ha un impatto sulla vita quotidiana sufficiente per giustificare il rischio di una terapia immunosoppressiva (se attiva) o chirurgica (se non è attiva).
- TED molto severa: paziente con neuropatia ottica distiroidea e/o ulcere corneali. Questa categoria richiede un intervento immediato.
Gestione della patologia
Una volta definita la TED e le sue caratteristiche cliniche, analizziamo come vanno gestiti questi pazienti. Nei pazienti con malattia di Graves conclamata, va sottolineata la possibilità dell’insorgenza dell’oftalmopatia tiroidea. È opportuno sottoporli ad indagini mirate periodiche che comprendono:
- Visita oculistica completa
- Esoftalmometria
- Valutazione della dinamica palpebrale
- Valutazione della motilità oculare
- Tavole di Ishihara (utili per valutare discromatopsia e sensibilità al contrasto)
- Esami ematochimici comprendenti fT3, fT4, TSH, TRab
- Campo visivo
Va sottolineata l’importanza della cessazione del fumo, il mantenimento dell’eutiroidismo ed il rischio che questi pazienti incorrono dopo terapia con iodio radioattivo (RAI).
La terapia viene di seguito riassunta dall’EUGOGO, sempre considerando i criteri CAS sul come intervenire.
Da notare come anche nella forma lieve i corticosteroidi, qualora indicati, sono endovenosi. La via di assunzione orale ha scarsa efficacia in questa patologia. La terapia antinfiammatoria steroidea ha un ruolo importante soltanto nelle forme attive (CAS maggiore o uguale a 3) e favorisce un miglioramento dei segni infiammatori, riduce parzialmente l’esoftalmo ma non migliora la diplopia (che vede come unica soluzione la chirurgia).
La chirurgia va valutata unicamente nelle forme non attive e prevede un lungo iter a step, fra i quali devono intercorrere almeno 6 mesi per favorire un’adeguata guarigione e il riassestamento dei volumi orbitari. Concretamente, nell’ordine prevede:
- Chirurgia orbitaria: decompressione con rimozione di componente ossea e di grasso
- Chirurgia dei muscoli estrinseci dell’occhio per correggere la diplopia
- Chirurgia palpebrale per risolvere la retrazione
Gli unici casi in cui si deve intervenire anche in patologia in fase attiva è durante una DON o per la presenza di ulcere corneali.
